真实病例:晚期肺腺癌PFS获益超过1年,依沃西单抗有望全面覆盖驱动基因阴性晚期NSCLC治疗
医脉通 2025.07.29

免疫2.0时代 实例先锋
12条内容
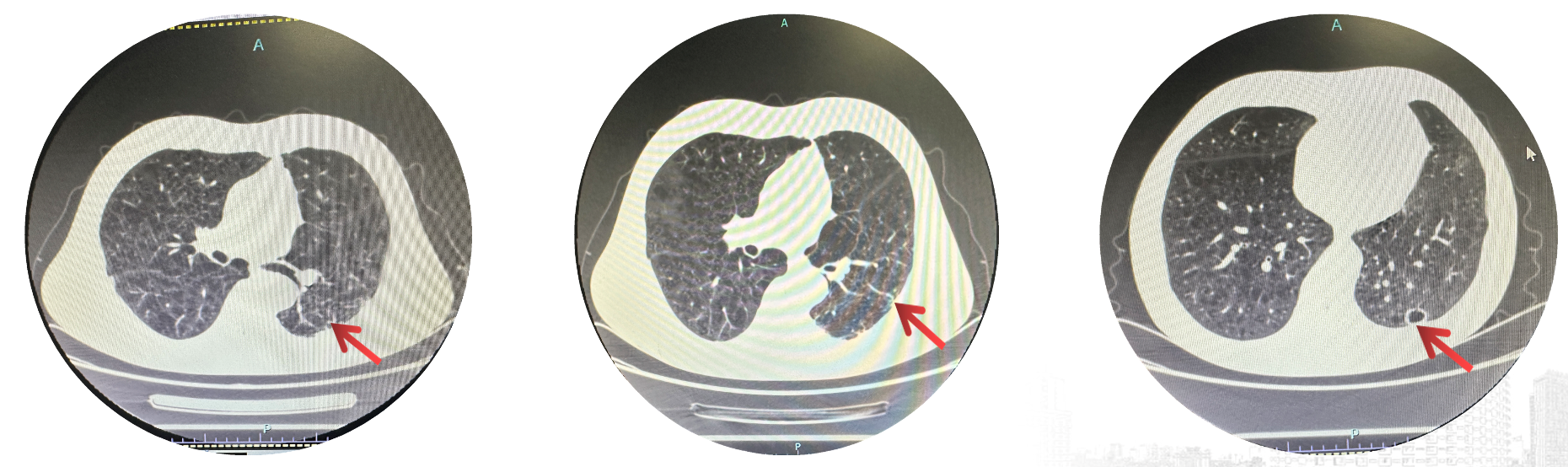
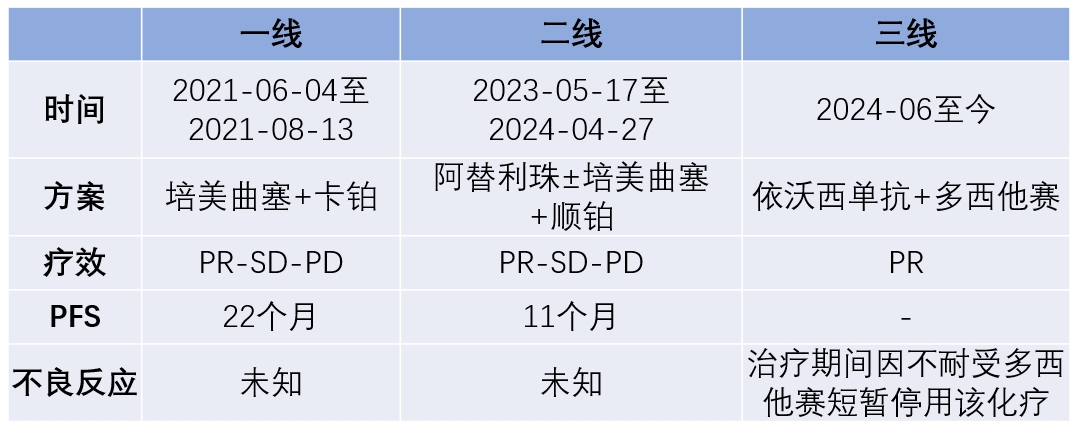
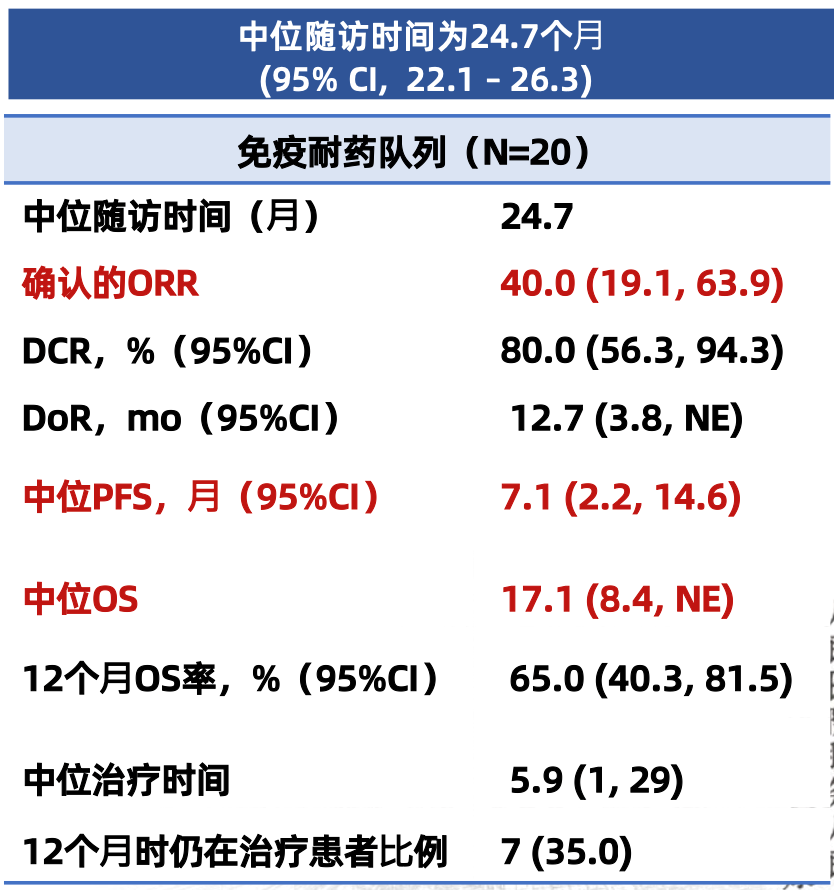
目前,免疫治疗已成为驱动基因阴性晚期NSCLC患者的一线标准治疗模式。随着免疫治疗在临床实践中深入应用,其疗效瓶颈逐渐显现,免疫治疗策略升级已成为进一步探索的重要方向。近年来,依沃西单抗作为“靶免一体”的双特异性抗体,能同时阻断血管生成-免疫检查点双通路,已在肺癌领域积累AK112-201、HARMONi-2[1~3]等研究探索成果,成为升级驱动基因阴性晚期NSCLC现有治疗策略的重要选择。 一例驱动基因阴性、PD-L1阴性晚期NSCLC患者,术后接受单纯化疗和免疫治疗联合化疗治疗;疾病再次进展后接受依沃西单抗联合多西他赛治疗,肿瘤迅速缓解,并实现无进展生存期(PFS)超1年。该病例由河南省人民医院曹志坤教授分享,河南省人民医院魏立教授结合该病例及研究进展进行深度点评,并探讨依沃西单抗全面覆盖驱动基因阴性晚期NSCLC患者的应用潜力,为该类患者患者诊疗临床实践带来重要启示。 患者男,63岁,因“肺恶性肿瘤综合治疗3年余”于2024年5月入院。患者既往于 ▪ 2021年4月27日行"胸腔镜下左肺上叶前段切除术、左肺下叶楔形切除术、左侧胸膜活检术及胸膜粘连烙断术",术后于2021年4月30日-5月5日行经皮热灌注治疗。 ▪ 2023年4月26日PET-CT复查提示:左肺新发多处结节;原左肺下叶胸膜下小结节较前增大伴代谢增高;左侧胸膜多发结节状、斑片状增厚伴代谢增高,考虑多发肺及胸膜转移瘤;左侧锁骨区新发淋巴结伴代谢增高,考虑淋巴结转移。 ▪ 2021年6月4日-8月13日完成培美曲塞+卡铂方案一线化疗。 ▪ 2023年5月17日至2024年4月27日行阿替利珠单抗±培美曲塞±顺铂方案二线治疗。 为寻求进一步治疗方案,患者再次入院。 影像学检查 2024年5月23日胸部CT显示:左肺呈现术后改变,左侧胸腔内见少量积液。左余肺胸膜下可见数个不规则结节影,其中较大者直径约16×12mm。左余肺内见一空洞病灶,壁厚薄不均,范围约15×14mm。双肺(左余肺及右肺中叶)散在分布微小结节影,直径约3-4mm。双肺呈现气肿改变,伴肺大疱形成。左余肺内可见钙化灶。左侧胸膜呈不均匀增厚,局部伴钙化改变。 图1 2024-05-23基线胸部CT图像 2024年6月17日头部MRI检查结果提示:双侧额叶散在缺血/梗塞灶,必要时增强检查;轻度脑白质病;轻度脑萎缩。 肿瘤标志物 癌胚抗原(CEA):10.21 ng/mL(↑,正常值<4.1 ng/mL)。 病理学检查 病理:肺浸润性腺癌。 基因检测 KRAS突变:p.Q61H,TPS<1%。 体格检查 ▪T 36.8°C,R 20次/分,P 80次/分,BP 120/80mmHg。 ▪ Karnofsky功能状态评分(KPS)为80%。 肺恶性肿瘤-肺浸润性腺癌(T4N3M1期) 2024年6月-2024年8月期间,患者接受依沃西单抗+多西他赛三线治疗,共完成4个周期。 2024年9月2日复查胸部CT:左肺术后改变,左侧胸腔少许积液。左余肺胸膜下可见数个不规则结节影,较大者范围约为16×12mm。另左余肺可见空洞,壁厚薄不均,范围约为15×14mm。左余肺及右肺中叶可见微小结节影,大小约为3-4mm。双肺气肿、肺大疱。左余肺可见钙化灶。各级支气管及其主要分支未见明显狭窄。左侧胸膜不均匀增厚,左侧胸膜局部钙化。疗效评估:部分缓解(PR)。 图2 2024-09-02胸部CT图像 治疗期间,患者对多西他赛出现不耐受,遂暂停治疗。 2024年11月18日起患者单独接受依沃西单抗治疗1个周期,以维持疾病控制。 2024年2月4日患者再次尝试多西他赛联合依沃西单抗治疗6个周期。截至2025年7月4日,患者病情稳定,疗效评估仍为PR。目前,患者仍在持续随访中。 本病例为老年男性患者,因“肺恶性肿瘤综合治疗3年余”入院,通过检查后初步诊断为“肺部恶性肿瘤pT4N3M1”,病理确诊为肺浸润性腺癌,基因检测提示KRAS p.Q61H突变、TPS<1%。该患者初步治疗行“胸腔镜下左肺上叶前段切除术、左肺下叶楔形切除”后采用培美曲塞联合卡铂方案化疗,一线PFS为22个月;疾病进展(PD)后,二线调整为阿替利珠单抗±培美曲塞±顺铂方案,二线PFS为11个月;再次PD后,三线采用依沃西单抗+多西他赛方案,治疗4个周期后即达PR,且治疗期间未出现明显免疫治疗相关不良反应(irAE)。 表1 病例小结 本病例为一例携带KRAS Q61H突变、PD-L1阴性(TPS<1%)晚期肺腺癌患者,尽管患者存在KRAS Q61H突变,但因缺乏标准靶向治疗,其一线治疗参考驱动基因阴性晚期NSCLC患者用药。尽管患者一线培美曲塞+卡铂化疗以及二线阿替利珠单抗±培美曲塞±顺铂治疗为患者带来PFS的延长,但疾病再度进展后如何制定治疗方案以提升患者生存获益成为难点。 PD-1/VEGF双特异性抗体—依沃西单抗凭借其“靶免一体”创新结构及独特的作用机制,为驱动基因阴性晚期NSCLC免疫治疗升级提供重要选择。AK112-201研究是一项开放标签、多中心、Ⅱ期临床研究,旨在评估依沃西单抗联合化疗在晚期NSCLC患者中的疗效及安全性。其EGFR/ALK阴性晚期NSCLC免疫经治队列(队列3)结果显示:在20例可评估患者(鳞癌7例,非鳞癌13例)中,客观缓解率(ORR)达到40%,疾病控制率(DCR)为80%,中位缓解持续时间(DoR)为12.7个月;同时,mPFS为7.1个月,mOS达17.1个月,12个月OS率为65%[1-2]。上述结果提示,依沃西单抗联合化疗治疗驱动基因阴性晚期NSCLC免疫经治患者取得高效且持久的肿瘤缓解的同时,也展示出明确的生存获益趋势。 表2 AK112-201研究队列3数据汇总 基于依沃西单抗AK112-201研究探索成果,经多学科团队讨论评估后,病例中患者自2024年6月起接受依沃西单抗联合多西他赛治疗。治疗期间,患者仅接受4个周期治疗即达PR, 2024年9月2日复查胸部CT显示,左肺下叶空洞实性成分减少,提示依沃西单抗联合多西他赛对局部病变具有明确的缓解作用。尽管患者因不耐受多西他赛而暂停治疗,但通过调整治疗方案(依沃西单抗单药),病情持续稳定,疗效维持在PR状态。这充分表明依沃西单抗在疾病控制中发挥了核心作用,且治疗过程中患者未出现明显irAE,展现出对依沃西单抗±化疗方案良好耐受性。该疗效与AK112-201研究中依沃西单抗所展现的肿瘤迅速缓解及良好安全性高度一致。截至最新随访时,患者三线治疗所带来的持续疾病缓解超1年。目前,患者仍在持续治疗中,有望继续从依沃西单抗方案中获益。 值得注意的是,尽管本病例中依沃西单抗联合多西他赛应用已处于三线,仍展现出显著且持久的肿瘤缓解以及良好的耐受性。我们不禁思考:若该驱动基因阴性、PD-L1阴性晚期NSCLC患者一线治疗中即使用依沃西单抗联合化疗治疗,是否能为患者带来更大的生存获益?AK112-201研究EGFR/ALK阴性晚期NSCLC初治队列(队列1)带来重要启示。其结果显示:在44例可评估患者中,cORR为53.5%,DCR高达 93.0%,mPFS未达到[1,3]。“早用早获益”这一设想的进一步明确,有望使依沃西单抗为驱动基因阴性、PD-L1阴性晚期NSCLC患者带来多线获益。值得一提的是,依沃西单抗在驱动基因阴性、PD-L1阳性晚期NSCLC探索中取得突破性进展。在该领域首个单药头对头对比帕博利珠单抗取得阳性结果的Ⅲ期临床试验—HARMONi-2研究中,依沃西单抗对比帕博利珠单抗可降低49%疾病进展或死亡风险(HR=0.51,P<0.0001)。综上可见,依沃西单抗作为划时代的新型免疫治疗药物,有望全面覆盖驱动基因阴性晚期NSCLC患者,同时展现出更为广阔的探索方向和应用空间,为肺癌患者免疫治疗获益开拓了更多可能。未来,期待依沃西单抗在驱动基因阴性晚期NSCLC治疗研究中持续探索,为我国肺癌患者全面开启免疫治疗2.0时代。 病例点评专家 魏立 教授 外科学部主任,胸外科主任,二级教授 医学博士,教授,博士生导师 享受国务院特殊津贴专家 河南省中原科技创新人才 河南省人民医院外科学部主任 河南省人民医院胸外科主任 河南省人民医院肺移植中心主任 国家卫健委胸外科质量控制中心专家组成员 国家卫健委肺移植质量控制中心专家组成员 中国康复医学会外科快速康复分会主委 河南省医学会胸外科分会主任委员 河南省医学会器官移植分会副主任委员 病例分享专家 曹志坤 教授 主任医师 河南省人民医院胸外科主任医师 医学硕士 河南省临床肿瘤学会食管癌专业委员会委员 河南抗癌协会食管癌专业委员会委员 河南省抗癌协会肺癌专业委员会委员 康复医学会外科加速康复委员会委员 参考文献: 1、Zhao Y, Chen G, Chen J, et al. AK112, a novel PD-1/VEGF bispecific antibody, in combination with chemotherapy in patients with advanced non-small cell lung cancer (NSCLC): an open-label, multicenter, phase II trial. EClinicalMedicine. 2023;62:102106. Published 2023 Aug 3. 2、Z. Li, et al. Phase II results of ivonescimab (ivo) a novel PD-1/VEGF bispecific in combination with chemotherapy for first-line treatment of patients (pts) with advanced/metastatic squamous (Sq) non-small cell lung cancer (NSCLC). 2024 ELCC, 68P. 3、Yuangyuan Zhao, et al. A phase II study of AK112 (PD-1/VEGF bispecific) in combination with chemotherapy in patients with advanced non-small cell lung cancer. 2022 ASCO, Abstract# 9019.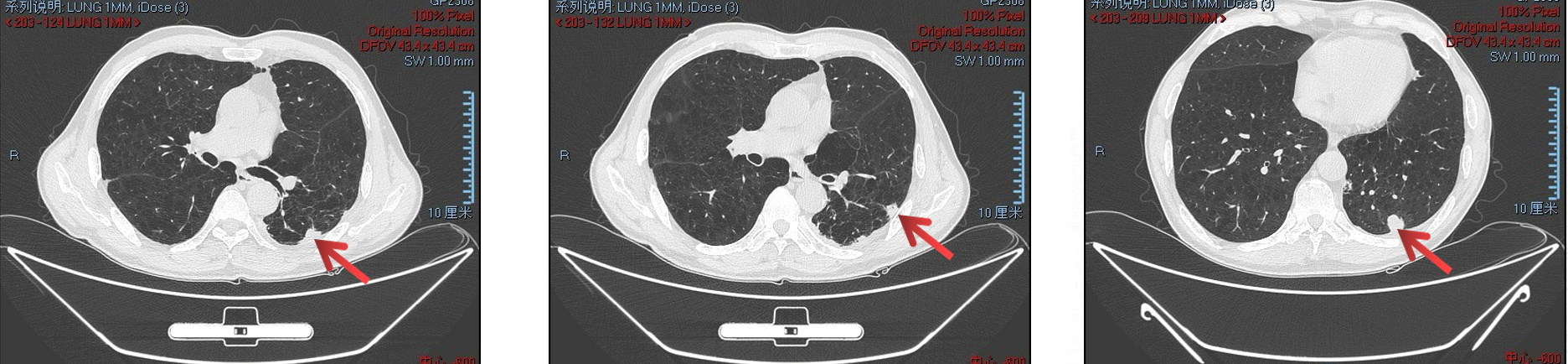
4