GI医声 第11期 I “靶”握未来,精准施治,靶向治疗助力结直肠癌患者更优获益
医脉通 2024.01.09

GI 医声
13条内容

导读:结直肠癌是我国一种常见的恶性肿瘤,大多数确诊时已经是中晚期。对于中晚期结直肠癌,药物治疗十分关键。化疗的疗效已进入平台期,分子靶向治疗成为改善晚期结直肠癌预后的主要治疗手段。近两年,随着靶向治疗研究与基因分型相关研究的深入,更多靶向药物也为晚期结直肠癌患者带来更好的生存获益。本期GI医声特邀北京朝阳医院安广宇教授、哈医大肿瘤医院李志伟教授、山西省人民医院李红霞教授分享结直肠癌靶向治疗进展,以飨读者。

研究背景
瑞戈非尼是一种多靶点小分子酪氨酸激酶抑制剂,目前已在全球多个国家和地区被批准用于转移性结直肠癌(mCRC)患者的三线治疗。既往较少有研究报道KRAS突变对瑞戈非尼疗效的影响。仅一项研究报告了接受瑞戈非尼治疗的存在高浓度循环游离DNA(cfDNA)的患者预后不良。本项研究评估了组织或血浆样本中KRAS突变和cfDNA浓度对瑞戈非尼治疗mCRC患者预后的影响1。
研究方法
这是RECC研究的一项生物标志物探索,评估了瑞戈非尼剂量递增治疗mCRC的疗效。血浆样本是在瑞戈非尼治疗开始前获得的。研究采用组织和血浆样本评估KRAS突变。从血浆样品中提取cfDNA进行定量检测。
研究结果
这项生物标志物研究共纳入了45例患者。组织样本中:无KRAS突变患者的中位无进展生存期(PFS)和总生存期(OS)分别为1.4个月(95%CI: 1.3-1.5)和6.8个月(95%CI: 5.0-8.5),有KRAS突变患者的中位PFS和OS分别为1.9个月(95%CI: 1.7-2.0)和8.9个月(95%CI: 6.5-11.2)。
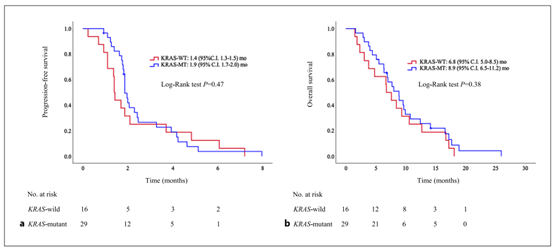
图1.组织样本中患者的PFS和OS结果
血浆样本中:无KRAS突变患者的中位PFS和OS分别为1.7个月(95%CI: 1.1-2.3)和8.9个月(95%CI: 6.7-11.2),有KRAS突变患者的中位PFS和OS分别为1.9个月(95%CI: 1.8-1.9)和7.0个月(95%CI: 5.3-8.7)。
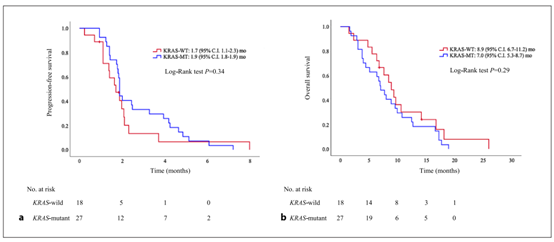
图2.血浆样本中患者的PFS和OS结果
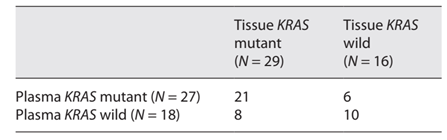
在瑞戈非尼给药前,45例患者中有29例在组织样本中检出KRAS突变(这29例患者中,血浆样本中有KRAS突变的21例)。16例组织样本无KRAS突变的患者中,6例(37.5%)在血浆样本中有KRAS突变。
表1.患者组织/血浆样本中的KRAS突变情况
DNA低浓度患者的中位OS显著优于高浓度患者(10.6个月vs.6.4个月,P=0.006),而二者的中位PFS无显著差异。
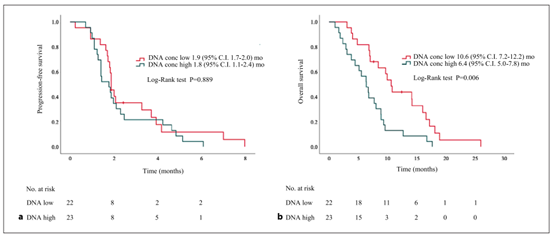
图3.不同DNA浓度患者的PFS和OS结果
研究结论
组织或血浆样本中的KRAS突变对瑞戈非尼的疗效没有影响。在后线化疗开始时,血浆中即可以检测到KRAS突变。高浓度cfDNA通常意味着接受晚期化疗的患者预后较差。
专家锐评

近年来,CRC发病率不断攀升。晚期CRC患者一线、二线治疗方案通常以氟尿嘧啶类药物为基础联合奥沙利铂或伊立替康,并依据基因状态添加抗VEGF或抗EGFR药物,三线用药目前国内有瑞戈非尼、呋喹替尼和TAS-102等。其中,瑞戈非尼是一种口服的多靶点小分子酪氨酸激酶抑制剂(TKI),可通过有效阻断VEGFR1-3、TIE2、RET、RAF1、KIT、BRAF、PDGFR和FGFR等多个蛋白激酶而发挥抗血管生成、抗肿瘤形成和改变肿瘤免疫微环境等功能2。
既往CORRECT和CONCUR研究显示,无论是否存在KRAS突变,患者均可从瑞戈非尼标准治疗中获得生存获益。本研究发现,组织或血浆样本中的KRAS突变对瑞戈非尼剂量递增治疗mCRC患者预后没有影响。此外,CONSIGN研究也发现,组织样本中KRAS突变对瑞戈非尼的疗效没有影响。仅Tabernero等的研究评估了血浆样本中KRAS突变对瑞戈非尼疗效的影响,并得出KRAS突变对瑞戈非尼疗效没有影响的结论。除了上述发现以外,研究还提示KRAS突变的出现可能是因为两个原因:空间异质性以及抗肿瘤药物导致的时间异质性。据报道,结直肠癌是分子异质性肿瘤,KRAS突变状态在原发肿瘤与转移肿瘤之间的一致性约为10%(空间异质性),抗EGFR药物可诱导KRAS突变“从头获得”。除KRAS突变外,其他原因也会导致抗EGFR治疗产生获得性耐药(如BRAF或EGFR突变)。另外,在接受化疗的患者中,DNA浓度随着疾病进展而增加。高浓度cfDNA通常意味着接受晚期化疗的患者预后较差1。
此次研究评估了组织或血浆中KRAS突变和cfDNA浓度对mCRC患者预后的影响。期待未来开展更大样本量的研究,以解答更多结直肠癌领域的相关问题。

研究背景
DEEPER研究评估了mFOLFOXIRI(伊立替康150 mg/m2,奥沙利铂85 mg/m2,5-FU 2400 mg/m2)联合西妥昔单抗(cet)对比贝伐珠单抗(bev)作为RAS野生型mCRC患者初始治疗的疗效。主要终点为肿瘤缓解深度(DpR),结果显示cet组具有更优的DpR。此外,在RAS/BRAF野生型和左半肿瘤患者中观察到cet组具有更长的无进展生存期(PFS)和总生存期(OS)。因此,通过肿瘤组织生物标志物分析,研究者使用更新的BRAF状态进行了生存分析3。
研究设计
研究纳入359例患者,其中255例 (71%) 患者的BRAF突变状态可进行生物标志物分析。在生物标志物研究中能够获取肿瘤样本的患者,利用二代测序或IHC评估其BRAF突变状态。

图1. DEEPER研究的研究设计
研究结果
178例RAS/BRAF野生型和左半肿瘤患者中,cet组的DpR和PFS显著优于bev组(中位DpR 59.2% vs 47.5%,P=0.0017;中位PFS 14.5个月 vs 11.9个月,HR 0.71,P=0.032)。
表1.更新分析结果(肿瘤缓解)
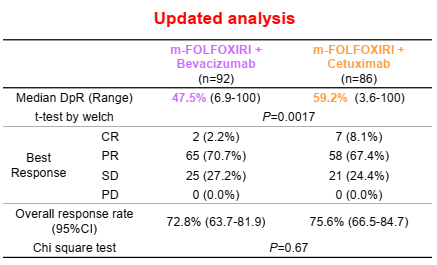
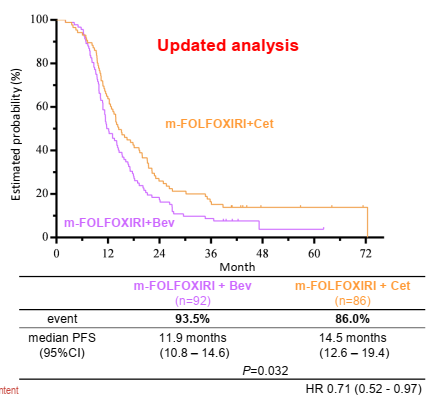
图2. 更新分析结果(PFS)
根据临床因素的亚组分析显示,cet组未行R0/R1手术切除的患者PFS更优(13.1个月 vs 11.1个月,HR 0.66,P=0.029),非肝转移患者PFS显著延长(15.1个月 vs 11.4个月,HR 0.63,P=0.015)。
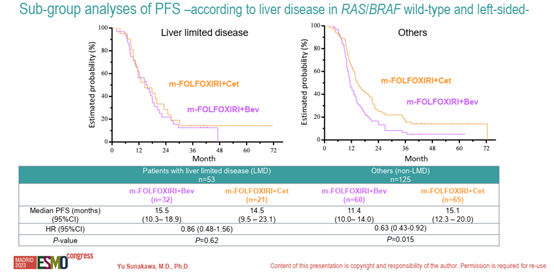
图3. 更新分析结果(PFS亚组)
研究结论
mFOLFOXIR联合cet方案对于RAS/BRAF基因野生型、左半mCRC患者来说,是一种具有高DpR、更长PFS的治疗选择。多发性或肝外转移患者也可能从中获益。
专家锐评

结直肠癌是我国常见恶性肿瘤,靶向治疗的出现使结直肠癌在药物治疗方面取得了较大进步。表皮生长因子受体(EGFR)单克隆抗体西妥昔单抗联合化疗是RAS野生型mCRC患者一线治疗的标准方案。据报道,西妥昔单抗使RAS野生型mCRC患者,尤其原发病灶位于左侧的患者在客观缓解率(ORR)、PFS和OS方面得到显著提高。但是不同于贝伐珠单抗,西妥昔单抗是否可用于RAS野生型mCRC患者一线治疗后维持治疗以及一线治疗进展后的后续治疗的问题仍值得探索。另外可以看到,化疗仍然是mCRC重要治疗选择。如何用好化疗药物以改善患者的生存依然非常重要3,4。
已有多项临床研究证明由氟尿嘧啶、奥沙利铂和伊立替康联合的FOLFOXIRI三药方案是一种治疗结直肠癌的高强度化疗方案,相比FOLFOX或FOLFIRI两药方案在结直肠癌患者中具有更好的疗效。然而,由于初始三药方案对患者耐受性要求也较高。近些年经过临床专家的不断摸索,创新性提出mFOLFOXIRI(modified-FOLFOXIRI)的用法和剂量(伊立替康150 mg/m2,奥沙利铂85 mg/m2,5-FU 2400 mg/m2)。2021年DEEPER研究显示,应用三药化疗联合西妥昔单抗能够获得更高的肿瘤退缩率,这对于为了手术而进行转化治疗来说至关重要。2023 ESMO会议上,DEEPER研究再次更新研究结果,证实了mFOLFOXIR联合cet方案对于RAS/BRAF基因野生型、左半mCRC患者来说,是一种较好的治疗选择。尤其是根据临床因素的亚组分析显示,cet组未行R0/R1手术切除的患者以及非肝转移患者的PFS更优;cet组男性较女性具有更佳PFS,男性接受cet治疗较bev具有更长的中位PFS。除此之外,中国版改良FOLFOXIRI(cmFOLFOXIRI)三药方案联合或不联合西妥昔单抗作为RAS/BRAF野生型不可切除的肝转移结直肠癌患者的转化治疗多中心、II期临床试验(FOCULM研究)也备受关注。该研究显示,与cmFOLFOXIRI单纯化疗相比,西妥昔单抗和cmFOLFOXIRI的方案联合治疗显著提高了初始技术上不可切除的BRAF/RAS野生型结直肠癌肝转移患者的NED率5。这些研究结果为三药化疗联合靶向药物在mCRC治疗中的临床应用提供了更多循证医学依据3。
相信随着更多新证据的出现和治疗优势人群筛选更加精准化,该策略可为合适的CRC患者争取更多治疗机会,并优化治疗策略和延长治疗的连续性,带来更多的生存获益。

研究背景
致癌基因KRAS G12C突变在结直肠癌(CRC)中约占3%,并且与不良预后有关。生物学原理支持抗EGFR治疗联合KRAS G12C抑制剂治疗该突变亚组人群。1b期CodeBreak101研究提示,sotorasib联合帕尼单抗治疗KRAS G12C突变的mCRC,ORR达到30%。
研究方法
CodeBreaK 300是一项全球多中心、随机对照、开放标签、主动对照研究,旨在评估KRAS G12C抑制剂sotorasib联合帕尼单抗用于标准治疗失败后的KRAS G12C突变型晚期CRC的疗效6。主要终点是盲法独立审查中心(BICR)根据RECIST 1.1评估的无进展生存期(PFS);关键次要终点包括总生存期(OS)、客观缓解率(ORR)等。
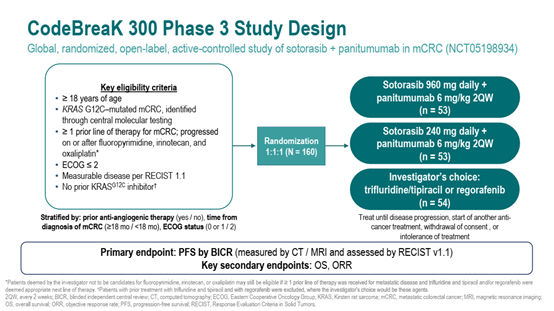
图1.研究设计
研究结果
在中位随访7.8个月后,Sotorasib 960mg+帕尼单抗组与Sotorasib 240mg+帕尼单抗组的中位PFS分别为5.6个月和3.9个月,标准治疗组为2.2个月。BICR评估的PFS在关键的亚组中,试验组均有获益。数据截止时OS数据尚不成熟。
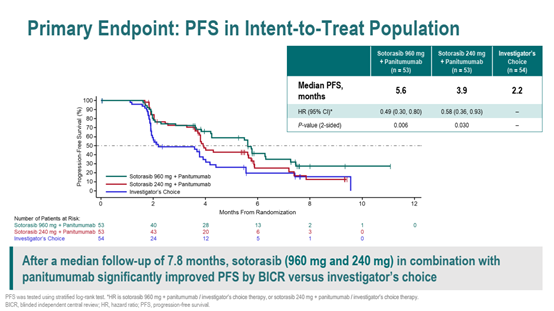
图2.主要终点PFS结果
Sotorasib 960mg+帕尼单抗组、Sotorasib 240mg+帕尼单抗组与标准治疗组的ORR分别为26%、6%和0%。DCR分别为72%、68%和46%。3组肿瘤退缩患者分别占81%、57%和20%。
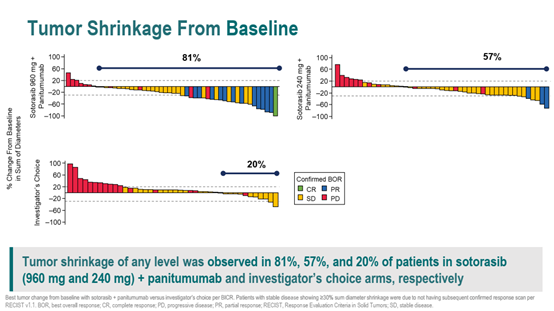
图3.不同治疗组患者的肿瘤退缩情况
安全性方面,Sotorasib 960mg+帕尼单抗组最常见≥3级治疗相关不良事件(TRAE)包括痤疮样皮炎、低镁血症和皮疹;Sotorasib 240mg+帕尼单抗组为低镁血症和腹泻;标准治疗组为中性粒细胞减少、贫血。
研究结论
在这项3期研究中,KRAS G12C抑制剂与EGFR抑制剂联合用于化疗难治性转移性结直肠癌患者,研究达到主要终点,无论Sotorasib 960mg+帕尼单抗组还是Sotorasib 240mg+帕尼单抗组,PFS均优于标准治疗组。并且Sotorasib 960mg+帕尼单抗和Sotorasib 240mg+帕尼单抗≥3级TRAE发生率较低,毒性可耐受。
专家锐评

结直肠癌是中国较为常见的恶性肿瘤。近年来,随着对结直肠癌发病机制的深入研究以及治疗新靶点的发现,针对特定靶点设计的相应药物有助于在个体化精准治疗的指引下延长结直肠癌患者尤其是难治性患者的生存期,并改善生活质量7。
KRAS G12C突变在结肠癌的发生率为1%~3%,且与患者预后不良有关。国外已上市的抑制KRAS G12C突变的小分子TKI如Sotorasib和Adagrasib在难治性晚期结肠癌中单药有效率可达10%~22%,实现了RAS突变型结肠癌靶向治疗的突破7。
CodeBreaK 300研究是KRAS G12C突变型肠癌领域第一个前瞻性、全球多中心随机对照研究,旨在评估KRAS G12C抑制剂sotorasib联合帕尼单抗用于标准治疗失败后的KRAS G12C突变型晚期结直肠癌的疗效。2023年,该研究结果登陆ESMO大会口头报告,同时全文在线发表于《新英格兰医学杂志》(NEJM)。CodeBreaK 300研究共分为3个组,两个治疗组分别探索不同剂量的sotorasib(960 mg及240 mg)联合标准剂量的帕尼单抗,对照组为标准三线治疗,主要目的是评估不同剂量的联合方案是否优于标准治疗,以及两个剂量组之间是否存在差异。结果显示,无论Sotorasib 960mg+帕尼单抗组还是Sotorasib 240mg+帕尼单抗组,PFS均优于标准治疗组,sotorasib联合帕尼单抗用于化疗难治性转移性结直肠癌患者的主要终点显示出阳性结果,且耐受性也较好6。CodeBreaK 300研究的成功,是该领域治疗获得突破进展的一个里程碑事件,也为这类晚期结直肠癌患者开辟了全新的治疗手段,其有望改变现有的临床实践。
经过多年探索,KRAS终于从“不可成药”靶点逆袭为“明星”靶点。未来,希望更多的新靶点也逐渐实现突破,从而造福更多患者。
参考文献
1.Ohta R, et al. Analysis of Circulating DNA to Assess Prognoses for Metastatic Colorectal Cancer Patients Treated with Regorafenib Dose-Escalation Therapy: A Retrospective, Exploratory Analysis of the RECC Trial. Digestion. 2023;104(3):233-242.
2.Wilhelm SM, et al. Regorafenib (BAY 73-4506): a new oral multikinase inhibitor of angiogenic, stromal and oncogenic receptor tyrosine kinases with potent preclinical antitumor activity. Int J Cancer. 2011;129(1):245-55.
3.Sunakawa Y, et al. Modified (m)-FOLFOXIRI plus cetuximab treatment and predictive clinical factors for RAS/BRAF wild-type and left-sided metastatic colorectal cancer (mCRC):the DEEPER trial (JACCRO CC-13) .2023 ESMO 555MO.
4.吴佳,周嘉梁. 西妥昔单抗在转移性结直肠癌一线治疗后的后续应用研究进展.中国癌症杂志, 2020, 30 (1): 64-69.
5.Hu H, et al. Modified FOLFOXIRI with or without cetuximab as conversion therapy in patients with RAS/BRAF wild⁃type unresectable liver metastases colorectal cancer: the FOCULM multicenter phase II trial.Oncologist.2020 26(1):e90⁃e98.
6.Fakih MG, et al. Sotorasib plus Panitumumab in Refractory Colorectal Cancer with Mutated KRAS G12C. N Engl J Med. 2023 Oct 22. doi: 10.1056/NEJMoa2308795.
7.中国医师协会结直肠肿瘤专业委员会, 中国抗癌协会大肠癌专业委员会, 国家癌症中心国家肿瘤质控中心结直肠癌质控专家委员会. 结直肠癌靶向治疗中国专家共识. 中华普通外科学文献(电子版), 2023, 17(1): 1-8.
